據西安中天生物廠家了解,2016年9月和2017年6月,CFDA分別發布了第一批和第二批過度重復藥品目錄。第一批公開了獲批準文號數大于20家企業的品種282個,第二批公開293個。
盡管第二批目錄比第一批品種數量增加,但對比兩批目錄中的相同品種,大部分品種的批文數量和擁有批文的企業數出現下降,僅個別品種出現少量的增加。尤其以氯化鈉、葡萄糖、甲硝唑、維生素C等大輸液品種的批文數量下降較多。
在銷批文數量變化程度較小,就目前而言,一致性評價的影響對過度重復藥品的數量影響程度較小。對比在銷批文數量變化,排除過度重復藥品的統計口徑的誤差之外,不難看出,批準文號數量和批準企業數量的減少,主要原因可能是“僵尸”批文或企業的消失。
對比國產和進口品種的銷售額分布情況,過10億元進口單品數量占進口單品總數的比例為4.2%,國產品種的這一比例僅為0.5%;銷售額在1億~10億元之間的進口單品比例則達到23.9%,國產品種這一比例僅為4.7%;單從銷售額維度,也可以看出國產品種與進口品種的巨大差異。
西安中天生物廠家表示:從以上分析可以看出,整體上現階段國產品種和進口品種仍存在較大差距,國產品種仍呈現出“多且不精”的特點,也就是我們常說的“低水平重復”。
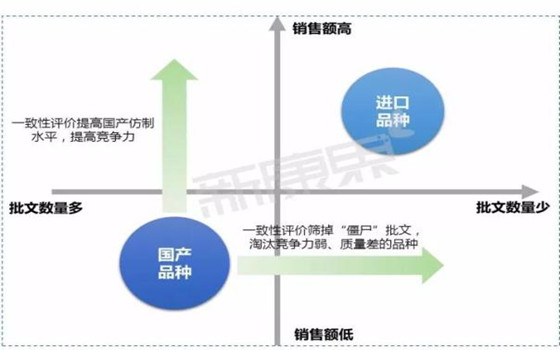
西安中天生物廠家表示:隨著仿制藥一致性評價工作的開展,“僵尸”批文、質量較差、競爭力弱的產品逐漸被篩除,具備更強競爭力的國產品種則被留下。不難想象,未來3到5年將會有越來越多的國產品種將與進口品種開展正面交鋒,國產替代進口的時代將真正到來。